Вы точно человек?
Оформи сейчас! Использование системно - деятельностного подхода в обучении, в сочетание с современными образовательными технологиями способствует формированию у школьников компетенции «учебная самостоятельность», получению высоких результатов в обучении. Чтобы пробудить у учащихся познавательный интерес на своих уроках химии, я создаю проблемные ситуации, «преодолимые трудности», решая и преодолевая их, учащиеся выполняют учебные действия, структурируют материал, выстраивают причинно-следственные связи. Чтобы облегчит путь познания и увеличить темп изучения материала без перегрузки обучающихся, я использую «опорные конспекты». Опытом их применения я и хочу поделиться. Приведу пример урока по теме «Оксиды» с использованием учебника «Химия — 8» авторов Г.





Самовывоз 1. Пункты выдачи заказов Boxberry 1. Пункты выдачи заказов «СДЭК» 1.
- Вход на сайт
- Одним из приемов реализации принципов обучения, в частности принципа системности и последовательности, является так называемая система В. Шаталова, в основу которой положены опорные конспекты схемы, сигналы.
- Приказ N
- Учителя химии широко начали их использовать после статей и книг математика В. Опорные конспекты хорошо обобщают материал, приводя его в систему, вскрывают причинно-следственные связи между понятиями, придают наглядность изложению.
- Системно-деятельностный подход в обучении с использованием опорных конспектов
- Книжные памятники Свет. Обратная связь Добавить в закладки Версия для слабовидящих Войти.
- Отправьте статью сегодня! Журнал выйдет 7 сентября , печатный экземпляр отправим 11 сентября.
- Уточнить адрес.



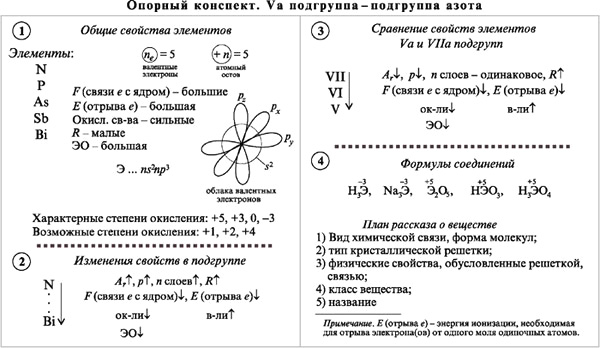









Страница 1 В целях интенсификации процесса обучения в ходе проведения лекции по теме учителем совместно с учащимися составляются опорные конспекты. Элементы главной подгруппы VI группы халькогены Строение внешнего энергетического слоя атомов элементов этой подгруппы следующее: О, S — ns2, np4; Se, Те, Ро - n — 1 d10, ns2, np4. В общем виде ns2, np4. При переходе в возбужденное состояние у всех атомов халькогенов кроме кислорода может увеличиваться число неспаренных электронов за счет перехода электронов с ns- и nр- подуровней на свободный nd-подуровень. При этом проявляются следующие валентные состояния.